Les maladies inflammatoires chroniques de l’intestin (MICI) (Inflammatory Bowel Disease, IBD), la maladie de Crohn et la Colite ulcéreuse, représentent une proportion de plus en plus fréquente de patients dans une consultation de gastroentérologie, ambulatoire ou hospitalière.
La gestion de ces maladies requiert de plus en plus d’expertise en raison de la multiplicité des présentations cliniques, des interactions avec d’autres maladies inflammatoires (Spondylarthrites, psoriasis, polyarthrites, sclérose en plaques, …), de leurs traitements et de leurs effets secondaires, des conditions d’optimalisation et de remboursements de leurs traitements, chez des individus souvent jeunes. Elle est d’ailleurs devenue une des 6 sous-spécialités de la gastroentérologie au même titre que l’oncologie digestive, les maladies fonctionnelles, l’hépatologie, l’endoscopie thérapeutique et la gastroentérologie générale.
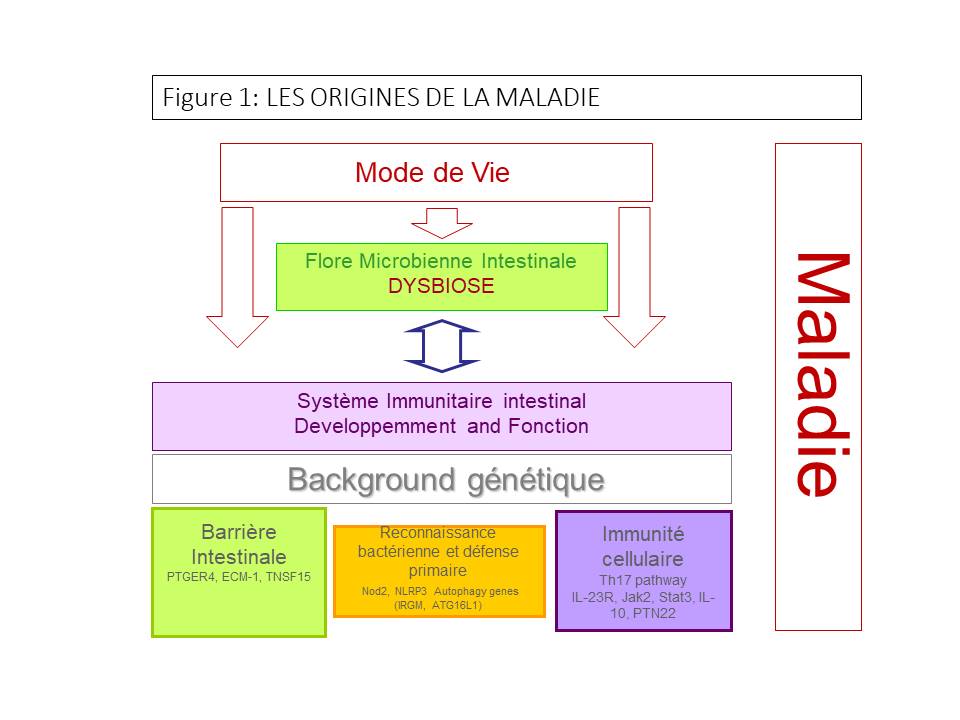
L’incidence de ces maladies n’a cessé d’augmenter de manière exponentielle (facteur de 2 à 10) ces 40 dernières années ; la prévalence des MICI est actuellement de 0.3 à 0.5% selon les régions du monde. Elles affectent essentiellement les jeunes dans la deuxième et troisième décade (Sex ratio Femme/ Homme 1.5) mais peuvent survenir à tout âge. Il s’agit d’une réelle épidémie mondiale liée à notre mode de vie occidentale (hygiène, alimentation, …) (Figure 1), puisque ces maladies sont moins fréquentes en Afrique, Asie ou d’autres parties du monde moins industrialisées. L’occidentalisation du moyen orient, comme les Emirats arabes et le Koweït, ou de la Chine a entrainé une forte augmentation de ces maladies dans ces pays. Ces maladies sont aussi des maladies héréditaires communes et plus de 200 gènes de susceptibilité ont pu être identifiés à ce jour. Ces gènes de susceptibilité codent pour l’intégrité de l’épithélium intestinal, des récepteurs de produits bactériens, et des composants de la réponse immunitaire adaptive. La compréhension de la maladie suggère qu’il s’agit d’une réponse inappropriée du système immunitaire digestif vis-à-vis de la flore microbienne chez un individu génétiquement susceptible. A la faveur d’un facteur environnemental (facteurs alimentaires, infections (bactéries, virus, parasites), turista, intoxication alimentaire, antibiotiques, anti-inflammatoires), la flore microbienne se modifie (elle devient dysbiotique : altération qualitative et quantitative de la flore microbienne) et va entrainer une rupture de tolérance du système immunitaire digestif déclenchant une réponse immunitaire poly-clonale vis-à-vis des composants de cette même flore microbienne, responsable de l’inflammation et destruction muqueuse à l’origine de la maladie (Figure 1).
Histoire naturelle de la maladie
La maladie de Crohn et la colite ulcéreuse évoluent de manière cyclique par phases d’activité ou poussées et rémissions cliniques, souvent sans facteurs déclenchants identifiés. A chaque cycle inflammatoire (sous formes d’érosions ou d’ulcères muqueux), la destruction tissulaire succède à l’inflammation et s’accompagne d’un remodeling tissulaire et de cicatrisation. La maladie de Crohn est une maladie inflammatoire segmentaire (qui peut affecter plusieurs segments de tout le tube digestif), de la bouche au canal anal, et transmurale (qui affecte toute la paroi du tube digestif). La colite ulcéreuse est une maladie inflammatoire uniquement du colon et est muqueuse et sous-muqueuse. Les complications de la maladie sont liées à cette destruction et remodeling tissulaire ; les complications dans la maladie de Crohn sont liées à l’apparition de sténoses (rétrécissements), ou de fistules ou d’abcès intra-abdominaux ou périnéaux, mais aussi au développement de maladies sévères réfractaires aux traitements et à la survenue de cancer comme dans la colite ulcéreuse.
Prise en charge et stratégie de traitements
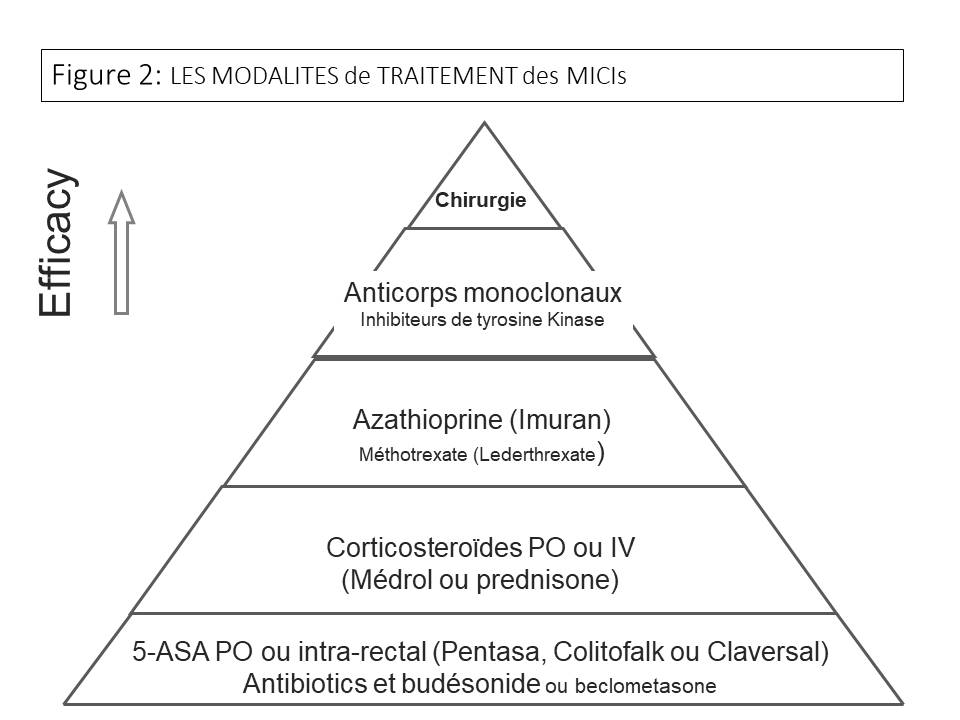
La prise en charge clinique, biologique, radiologique et endoscopique débute au diagnostic (bien que des stratégies de prévention prendront bientôt naissance) et s’étend tout au long de la vie de l’individu que ce soit dans la prévention ou le traitement des complications. Il n’existe pas encore de traitement curatif mais il existe de nombreuses stratégies de traitements dont l’objectif maintenant largement reconnu est la cicatrisation muqueuse complète. L’arsenal thérapeutique est en constante évolution et inclut (outre les dérivés de mésalamine, les corticostéroïdes topiques et systémiques, et les immunosuppresseurs conventionnels) un nombre croissant d’anticorps monoclonaux, et de « small molecules » (inhibiteurs de kinases) (Figure 2)
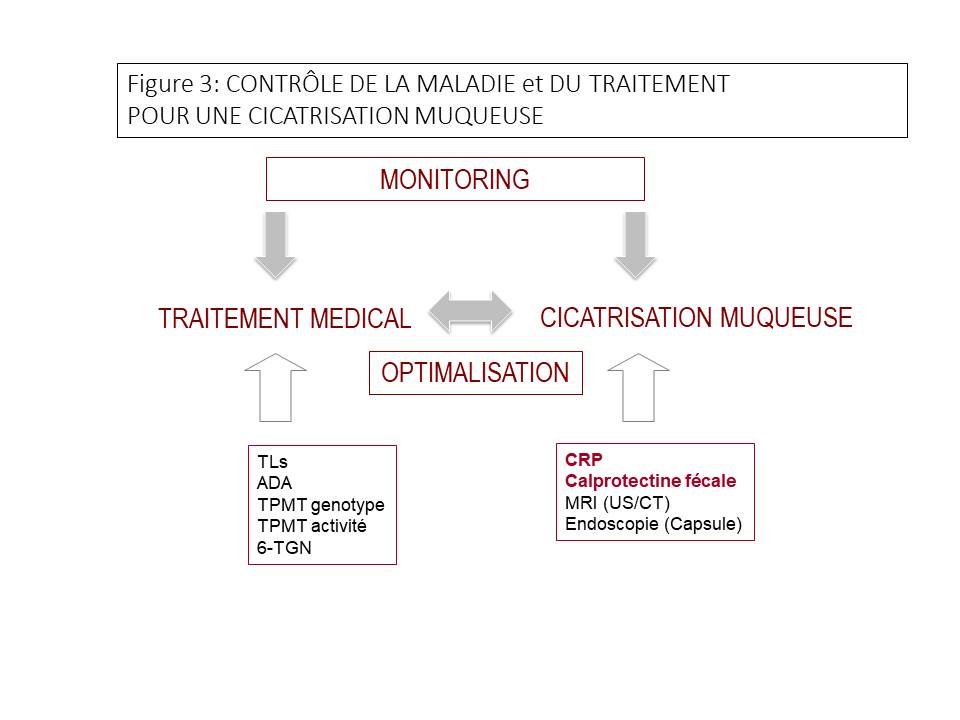
Les stratégies de traitements sont de plus en plus complexes en fonction de la localisation, du comportement, du stade, de l’évolutivité et de la sévérité de la maladie. L’objectif du traitement, la cicatrisation muqueuse complète, nécessite d’une part un monitoring des traitements grâce à différents marqueurs biologiques (comme les dosages sériques d’anticorps monoclonaux ou de leurs anticorps neutralisants) et d’autre part un monitoring de la maladie sur des critères biologiques, endoscopiques et radiologiques de manière à permettre une optimalisation continue des traitements (en mono- ou combo-thérapie) tout en prévenant leurs effets secondaires (Figure 3). Cette monitorisation de la maladie permet d’éviter également le développement de complications et le dépistage et la surveillance du cancer colorectal.
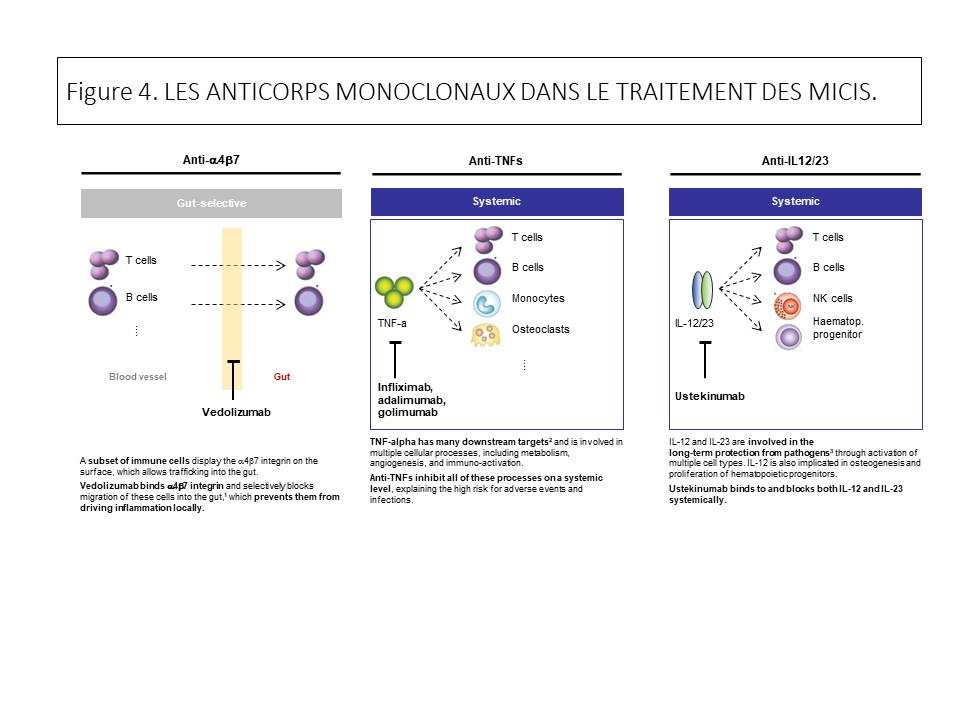
L’arsenal thérapeutique des MICIs (Figure 4) s’est considérablement enrichi au cours de ces dernières années du développement des anticorps monoclonaux utilisés aussi dans d’autres indications comme la spondylarthrite ankylosante, l’arthrite psoriasique, la polyarthrite rhumatoïde, le psoriasis et d’autres maladies auto-immunes ou auto-inflammatoires. A côté des dérivés de la mésalamine, des corticostéroides (topiques, oraux ou intraveineux) et des immunosuppresseurs conventionnels utilisés depuis les années 1970, la venue et le développement des anticorps monoclonaux a totalement révolutionné la prise en charge des patients avec maladie de Crohn et Colite ulcéreuse. Dès la fin des années 1990, il apparut rapidement que les anti-TNF, anticorps monoclonaux ciblant le TNF, un médiateur inflammatoire pivot de l’inflammation, comme l’infliximab (le Remicade (MSD) et l’Adalimumab (Humira (Abbvie), étaient associés à une plus grande efficacité sur l’induction et le maintien de la réponse (60%) et la rémission clinique (30%) que les traitements conventionnels, mais surtout permettaient une cicatrisation muqueuse des lésions muqueuses (endoscopiques) chez ces patients. Les patients qui présentaient une cicatrisation muqueuse développaient moins de complications, nécessitaient moins d’hospitalisations ou de recours à la chirurgie. Certains de ces patients présentaient même une rémission au long cours sans biologiques. Les anti-TNF en induisant une cicatrisation muqueuse précoce chez les patients nouvellement diagnostiqués pouvaient réellement changer l’histoire naturelle de ces maladies.
Aujourd’hui leurs modalités d’utilisation clinique et une meilleure compréhension de leur pharmacocinétique permet encore d’optimaliser leur efficacité. Toutefois, le facteur le plus limitant à leur utilisation est la perte de réponse secondaire (0-50% par an dépendamment du type de patients et de maladies) liée à l’immunogénicité (le système immunitaire du patient développe des anticorps neutralisant contre l’anticorps monoclonal) et le catabolisme (la destruction des anticorps monoclonaux par le système réticulo-endothélial du patient). La nécessité clinique de développer d’autres anticorps monoclonaux ciblant d’autres voies de l’inflammation s’est vite imposée pour tous les patients échappant aux anti-TNF. Depuis 2015, une nouvelle classe d’anticorps monoclonaux, les anti- molécules d’adhésion, s’est développée ciblant la recirculation des lymphocytes activés pathogéniques dans les MICIs. L’Entyvio (Takeda) ou vedolizumab neutralise la molécule d’adhésion intégrine alpha 4- Beta 7 exprimée sur lymphocytes activés pathogéniques, en empêchent ceux -ci de traverser les vaisseaux sanguins et de migrer au sein de la sous-muqueuse intestinale. L’Entyvio a également démontré son efficacité sur l’induction et le maintien de la réponse et la rémission clinique dans la colite ulcéreuse et la maladie de Crohn. Plus récemment en janvier 2017, le Stelara (Janssen) ou ustekinumab est remboursé comme traitement d’induction et de maintenance dans la maladie de Crohn et, depuis septembre 2020, dans la colite ulcéreuse. L’ustekinumab cible la sous-unité P40 de l’interleukine 12 et 23 dont le rôle est déterminant dans la différenciation et le développement des lymphocytes Th17 pathogéniques pour la muqueuse intestinale. Il est remarquable de constater que tous les composants de la voie de signalisation de l’IL-12 et de l’IL-23 sont des gènes de susceptibilité pour la maladie de Crohn. Aujourd’hui, une nouvelle classe d’anticorps monoclonaux, ciblant la sous-unité P19 de l’interleukine 23 comme le risankizumab (Abbvie), sont évalués en phase III et apparait d’une redoutable efficacité dans le contrôle du psoriasis et des MICIs. Jusqu’il y a peu, les indications des small molecules ou les inhibiteurs de kinases étaient réservés aux traitements des leucémies, et des tumeurs solides (GIST, carcinomes uro-épithéliaux, hépatocarcinome, adénocarcinome colorectal métastatique, …). Le Xeljanz (Pfizer) ou tofacitinib est un inhibiteur de Jak1 et Jak3 qui sont deux enzymes indispensables dans la signalisation de nombreux récepteurs cytokiniques qui interviennent dans l’inflammation. Le Xeljanz est un traitement efficace de la polyarthrite rhumatoïde et est remboursé depuis septembre 2019 dans le traitement de la colite ulcéreuse. Les conditions de remboursement et d’utilisation de chacun de ces traitements deviennent de plus en plus complexes et demandent une mise à jour constante. Il existe par ailleurs de nombreuses études cliniques en cours qui sont indispensables pour les patients muti-réfractaires en bout de traitement.
Parallèlement, les compagnies à l’origine des produits de référence comme le Rémicade (MSD) (Infliximab) et l’Humira (Abbvie) ont perdu leur licence d’exclusivité et de nombreux biosimilaires ont vu le jour. Dans les hôpitaux CHIREC, le Remsima (Cellltrion) remplace le Rémicade. Le prix a diminué de 60% ce qui représente une véritable économie pour l’INAMI et la sécurité sociale. Il existe de nombreuses autres compagnies de biosimilaires très dynamiques comme Pfizer pour l’inflectra et Biogen pour le Flixabi. Les compagnies de biosimilaires comme Cellltrion (préalablement Mundipharma) s’engagent à également participer à l’amélioration de pris en charge des patients au CHIREC. C’est aussi le cas également de la compagnie Amgen qui produit l’Amgevita, le biosimilaire de l’Humira.
Tous ces traitements ne sont pas interchangeables et sont indiqués en fonction du profil de la maladie (âge au diagnostic, localisation, comportement, activité (sévérité), progression (évolution), manifestations extra-intestinales, manifestations périnéales, maladies inflammatoires et auto-immune associées), le profil des traitements (efficacité, sécurité (effets secondaires, modes et intervalles d’administration, pharmacocinétique, cible pharmacologique (le voie de l’inflammatoire neutralisée par l’anticorps) et le profil du patient (âge, occupation professionnelle, profil psychologique, désirs personnels, …).
Les approches non pharmacologiques
De nouvelles modalités non pharmacologiques de traitements se développent telle que la transplantation fécale. La seule indication de la transplantation fécale aujourd’hui est la colite à clostridium difficile récurrente et résistante aux traitements antibiotiques (métronidazole et vancomycine). Il n’existe aujourd’hui que peu d’évidences scientifiques sur bases d’études randomisées pour proposer ce type de traitement dans les maladies inflammatoires chroniques de l’intestin. Beaucoup d’autres indications potentielles voient le jour comme dans l’obésité mais ne sont pas validées également. En effet, selon le conseil supérieur de la santé, son implémentation dans la pratique clinique nécessite qu’elle s’inscrive uniquement dans des protocoles de recherche. Ceci requiert d’abord l’élaboration d’une population de « super-donneurs » avec une caractérisation exhaustive clinique, biologique et microbiologique des donneurs et une caractérisation de leur flore microbienne par Next Generation Sequencing (NGS). Ce sont ces super-donneurs à la flore très diversifiée qui pourrait permettre de corriger de manière transitoire ou pérenne la dysbiose des patients souffrant de MICI. L’étude des super-donneurs et des patients receveurs nécessitent une conservation de leurs échantillons avant et après traitement pendant 30 ans. Ceci représente un challenge clinique, microbiologique, génomique et logistique durant les prochaines années. Ces travaux seront développés en collaboration avec l’Hôpital Erasme et l’ULB.
Il n’existe pas encore à l’heure actuelle de Régime spécifique des MICIs. Les recommandations internationales en nutrition dans les MICIs sont celles de la pyramide alimentaire. Il est vraisemblable qu’il existera à termes des recommandations dans la prévention et le traitement avec une meilleur compréhension du microbiote et d’immuno- phénotypes des patients. Madame Pauline Van Oytsel, diététicienne, qui consultera prochainement sur le site de l’hôpital DELTA, nous apportera une approche rationnelle scientifique dans la prise en charge diététique des patients avec maladie de Crohn et Colite ulcéreuse.
L’approche méditative apparait pertinente dans la prise en charge des patients MICI puisque le stress personnel, familial, professionnel ou social est responsable dans la colite ulcéreuse de 40-60% des poussées selon les études épidémiologiques. La pleine conscience est une pratique qui consiste à amener volontairement son attention sur notre expérience (pensées, émotions, sensations), et cela, de manière non jugeante et avec bienveillance. Des pratiques centrées sur le corps et les cinq sens sont proposées pour cet entraînement. Il ne s’agit pas d’une psychothérapie de groupe. Le programme comporte 8 séances hebdomadaires de 2h30 à 3h00 ainsi qu’une journée complète. Une pratique quotidienne d’environ 45 min sera à réaliser chez soi quotidiennement entre les séances à l’aide d’un support audio. Ce programme appelé, MBSR (Mindfulness-Based-Stress Reduction), élaboré en 1979 par John Kabat-Zinn, Université du Massachussets aux Etats-Unis, connaît un développement important depuis plus de 30 ans dans le monde entier. Il est proposé aujourd’hui par de nombreux hôpitaux à travers le monde et s’est particulièrement développé à l’hôpital de Braine l’Alleud -Waterloo et à l’hôpital DELTA grâce au Dr Olivier De Lathouwer et Mme Sybille de Ribaucourt. Les études scientifiques mettent en évidence son efficacité dans la réduction des symptômes anxieux et/ou dépressifs dans de nombreuses maladies chroniques comme la Maladie de Crohn et la Colite ulcéreuse. Il existe des bienfaits immédiats et évidents après quelques jours à quelques semaines sur notre anxiété, nos émotions, notre concentration et notre cognition. Les participants doivent s’engager fermement à être présent à chaque séance et à pratiquer quotidiennement tous les exercices à domicile. Les séances d’informations ont lieu avant chaque trimestre ou semestre. Elles sont obligatoires. Les dates, et les lieux où se dérouleront les prochains cycles sont communiqués séparément par feuillet (dans ce dépliant) ou par Email ou par le site internet : www.mindfullife.be. Ces cycles se donnent actuellement à Psy-pluriel (Institut Fond Roy), à l’hôpital de Braine-l’Alleud – Waterloo et à l’hôpital Delta. Les groupes durant les cycles sont mixtes. Il n’y a actuellement pas de groupes spécifiquement de patients souffrant de maladie de Crohn ou Colite ulcéreuse, sauf s’il y avait une demande de plusieurs participants. En d’autres termes, nul ne sait durant les cycles que le patient d’une maladie de Crohn ou Colite ulcéreuse (sauf si le patient souhaite partager cette information). Dans ces groupes, il y a d’autres patients souffrant d’autres maladies et des personnes qui ne sont pas malades.
Vers une voie de soin multidisciplinaire transversale multi-sites
La prise en charge des MICIs demande, comme dans beaucoup de domaines (oncologie, diabétologie, ..), une multidisciplinarité qui s’impose et se manifeste par besoin des médecins spécialistes en gastroentérologie, radiologie, chirurgie, et anatomopathologie de se concerter pour certains patients à la maladie complexe.
Une voie de soins se développe actuellement au CHIREC dans la prise en charge de ces patients. Les patients sont souvent jeunes et demandent beaucoup d’attention quotidienne, de réactivité immédiate et de patience de la part des praticiens pour une meilleure acceptation de la maladie (et des traitements) par le patient. L’interaction avec les médecins en charge des maladies inflammatoires dans d’autres spécialités comme surtout la Rhumatologie et la Dermatologie mais aussi et la Médecine interne, l’Ophtalmologie et la Neurologie sont quotidiennes. Cette voie de soins intègre aussi de manière centrale les spécialités paramédicales, comme la nutrition, la psychologie, la kinésithérapie, ou encore la stomathérapie. Cette voie de soins devient une démarche quotidienne inclusive et transversale sur tous les sites. Elle inclut chaque médecin qui a développé son expertise dans les maladies inflammatoires quelle que soit leur spécialité. Nous espérons très prochainement bâtir sur l’incroyable savoir faire des médecins du CHIREC et sur l’engagement d’une infirmière de coordination.
Pr. Denis Franchimont
Service de Gastroentérologie, Chef de Service – site Braine-l’Alleud, sites Delta et Braine-l’Alleud, CHIREC.
Consultation de Gastro-entérologie HBW : 02/434 70 90
Consultation de Gastro-entérologie DELTA : 02/434 81 05
Lire aussi:
– L’ntérêt du Fibroscan dans la prise en charge de la NASH en 2020
– Reflux: quand la PH-impédancemétrie œsophagienne s’impose
– Revue pratique d’un syndrome fréquent: le côlon irritable (IBS)
– Echoendoscopie interventionnelle: «une technique en pleine évolution»
– La Vidéocapsule endoscopique du grêle: pour qui, pour quoi ?